Screening oncologici e mammografia di screening.
Ieri abbiamo letto sui giornali che la Regione Veneto ha cambiato le regole sugli screening oncologici e in modo particolare sullo screening per la patologia mammaria. Ha deciso che la mammografia di screening può essere fatta solo se sintomatica sotto i 50 anni.

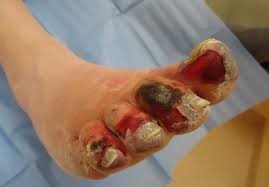
La mammografia aiuta nella dignosi
Cosa significa ?
Se una donna vuole fare una mammografia per vedere la sua situazione perchè ha paura , perchè può pensare di avere un tunore, magari perchè lo aveva la mamma, il medico non può farle la impegnativa. La donna dovrà pagare non il ticket ma l’esame completo

come si taglia lo screening
Molti si ricorderanno che non sono molti gli anni da quando nella nostra zona è partito lo screening mammografico per la diagnosi precoce del tumore al seno
Il sottoscritto aveva ideato nel 1992 uno screening artigianale che consiteva nella visita senologica del medico di famiglia che poi . se lo riteneva, prescriveva la mammografia.
Poi nel 2005 prese il via la mammografia di screening su base istituzionale . No stessi de Il Ponte abbiamo regalato alla ASL EURO 50.000 per la diffusione dello screening mammografico
Era noto che solo la mammografia può fare una diagnosi precoce mentre la ecografia e la visita clinica sono complemento alla diagnosi mentre la citologia o la microistologia definiscono la lesione.
La Regione scriveva ed era valido fino ad ora che gli screening oncologici sono importantissimi, esendo dimostrato in maniera statistica che una diagnosi precoce migliora i risultati chirurgici e medici del tumore mammaria , allungando di molto la vita
Riconosceva anche che il risparmio per lo Stato era significativo
Ora improvvisamente cambia
Riporto qui sotto
quanto ho copiato dal sito della Regione Veneto sia per quanto riguarda gli screening oncologici e sia per quanto riguarda lo screening mammografico
Noi avevamo lanciato il progetto ” Ama Il Tuo Seno ” e con piacere vedo che lo IEO ( Istiuto Europeo Oncologico ” di Milano ha nel suo programma il logo che io avevo messo per la nostra campagna di inoformazione

Programma di diagnosi precoce del tumore al Seno
E vediamo ora cosa dice la Regione Veneto
Screening oncologici
Nel 1996 sono state pubblicate le Linee Guida della Commissione Oncologica Nazionale sugli screening oncologici; i Piani Sanitari Nazionali successivi hanno dato indicazioni alle Regioni e alle Aziende Sanitarie per la realizzazione di programmi di screening oncologici organizzati.
I Programmi di screening oncologici in corso di attività sono attualmente tre: mammografico, citologico (cervice uterina) e colon-rettale.
Gli screening per il tumore della cervice uterina, della mammella e del colon retto sono stati inseriti tra i Livelli Essenziali di Assistenza con DPCM 29.11.2001.
Essi non possono assumere carattere discontinuo o a termine, la loro finalità è quella di ridurre la mortalità per neoplasia, in quanto il tumore viene riscontrato in una fase più precoce. I programmi di screening oncologici sono garantiti per la popolazione che rientra nelle caratteristiche di genere ed età stabiliti dalle Linee Guida della Commissione Oncologica Nazionale e successive integrazioni.
Ciascuna Azienda ULSS è responsabile della gestione dell’intervento sul territorio di propria competenza. In ciascuna Azienda ULSS è presente una segreteria organizzativa che invita il cittadino a recarsi presso la struttura sanitaria per eseguire il test previsto dallo screening.
Nel 2007 è stato approvato dalla Regione il Manuale per l’accreditamento istituzionale dei programmi di screening oncologici (DGRV 4538 del 28.12.2007) che determina i requisiti necessari per la qualità dei programmi attivi in ciascuna Azienda ULSS.
Tutti i programmi di screening possono avvalersi del Sistema Informatico regionale al fine di migliorare il servizio sanitario offerto, rendendolo più veloce, trasparente e sicuro.
Atti e documenti
Piano Nazionale Prevenzione 2010-2012
Piano Regionale Prevenzione del Veneto – anni 2010-2012 (D.G.R n. 3139/2010)
D.G.R n. 1235 del 16 luglio 2013: Recepimento dei documenti Ministeriali di sintesi delle più recenti evidenze scientifiche rispetto ad obiettivi di salute in particolare:”Documento di indirizzo sullo screening per il cancro della prostata, Documento di indirizzo sullo screening per il tumore del polmone con CT scan a bassa dose e il Documento di indirizzo sull’utilizzo del test HPV – DNA come test primario per lo screening del cancro del collo dell’utero”.
D.G.R. n. 2324 del 28 luglio 2009: Progetto per l’implementazione dell’applicazione software per la gestione dei programmi di screening oncologico (screening mammografico, citologico e del colon retto) da parte delle Aziende ULSS della Regione del Veneto. Trasferimento presso l’Unità Complessa Sistema Informativo Socio Sanitario della Direzione Risorse Socio Sanitarie del “Gruppo tecnico di gestione software regionale per lo screening oncologico”.
D.G.R. n. 4538 del 28 dicembre 2007: L.R. 16 agosto 2002, n. 22 – D.G.R. n. 2501 del 06/08/2004: – Approvazione del Manuale per l’accreditamento istituzionale dei programmi di screening oncologici delle strutture del Servizio Sanitario Regionale
D.G.R. n. 2605 del 07 agosto 2007: Sviluppo e promozione della qualità degli screening oncologici. Finanziamento di Programmi di Screening Aziendali e di Programmi di controllo e promozione della qualità. Impegno di spesa.
Approfondimenti e reportistica
Screening mammografico
Screening citologico
Screening colon-rettale
Altri screening oncologici
Rapporto Regionale Screening Oncologici 2013-2014 [pdf 5,13MB]
Link utili
Dipartimenti di Prevenzione delle ULSS del Veneto
Osservatorio nazionale screening
Screening oncologico mammografico
A questo screening sono invitate le donne tra i 50 e i 69 anni. È gratuito.
Lo screening mammografico prevede l’esecuzione del test mammografico ogni 2 anni, quale esame di primo livello. Qualora il test risultasse positivo o dubbio la donna verrà inviata all’esecuzione del secondo livello di approfondimento, per concludere l’iter diagnostico- terapeutico ed eseguire i controlli successivi opportuni.
I programmi di screening mammografico attivi nelle Aziende ULSS della Regione sono completi.
I dati europei presentati recentemente in letteratura (Suppl. Journal of Medical Screening; 9/2012), hanno confermato che lo screening mammografico organizzato è in grado di ridurre significativamente la mortalità per il tumore della mammella femminile.
Nel corso degli ultimi anni, nella Regione del Veneto vi è stata una progressiva dismissione delle apparecchiature radiologiche analogiche per le mammografie, che sono state sostituite da quelle digitali.
I vantaggi di questa evoluzione tecnologica sono molteplici, in particolare riguardano:
• la qualità delle immagini ottenute,
• la loro più agevole lettura
• la riduzione della dose di radiazioni erogata per prestazione
• la loro maggiore sensibilità e specificità
• aumento dell’efficacia dei programmi di screening.
Link utili
Dipartimenti di Prevenzione delle ULSS del Veneto
Osservatorio nazionale screening
Complessivamente la popolazione obiettivo da invitare a inizio 2014, costituta dalle donne residenti di età compresa tra i 50 ed i 69 anni, era pari a 645.126 donne. Un elevato numero di queste (71.987) sono state escluse dall’invito perché già affette dalla patologia, per aver effettuato spontaneamente il test di recente o per altri motivi. Pertanto nella Tavola 2 viene riportato il dato relativo all’estensione “corretta”, calcolata come il rapporto tra il numero di persone invitate ed il target su base annuale, costituito dal numero di residenti meno le donne escluse prima dell’invito. Anche se si registrano risultati diversi tra i singoli programmi, la maggioranza di essi ha riportato valori di estensione ottimali. Complessivamente, infatti, sono state invitate 284.153 donne, per un’estensione corretta su base annuale del 97,9%, un ottimo risultato che evidenzia come i programmi del Veneto siano riusciti a garantire l’offerta dello screening alla grande maggioranza della popolazione. E’ interessante valutare anche l’andamento dell’estensione su un periodo più lungo di un anno solare, poiché per diverse ragioni è possibile che i programmi non abbiano un andamento costante degli inviti, per cui un valore non ottimale ottenuto in un anno potrebbe venire compensato da quello dell’anno precedente. Quello che è fondamentale è che il programma sia in grado di invitare tutta la popolazione target nell’ambito del round cioè, nel caso dello screening mammografico, in due anni. La Figura 1 riporta le estensioni corrette degli inviti registrate nell’ultimo biennio 2013-2014. L’estensione corretta media ottenuta nel periodo è pari al 99,1%d . Si conferma che diversi programmi hanno un andamento degli inviti non del tutto omogeneo da un anno all’altro. Tuttavia, nella maggioranza dei casi il risultato complessivo è molto positivo, con soltanto un paio di programmi che non ha raggiunto un’estensione complessiva media dell’90%e . Si osservi come in molti casi l’incremento di estensione legato alla correzione dell’indicatore è rilevante: questo è un segno dell’efficacia del lavoro di pulizia delle liste che viene effettuato dalle segreterie dei programmi e si traduce in una maggiore efficienza degli inviti, i quali vengono rivolti ad una popolazione meglio selezionata e quindi con maggiori probabilità di risposta all’invito. Da sottolineare il caso dell’ULSS 14, dove la quota di donne invitate nel 2014 raggiunge il 143% a fronte del 54% dell’anno precedente: questo forte sbilanciamento degli inviti è dovuta alla particolare suddivisione del territorio ed alla relativa organizzazione degli inviti, per cui un anno vengono invitati i comuni di Cavarzere e Cona, e l’anno successivo quello di Chioggia dove si concentra più di due terzi della popolazione, raggiungendo alla fine del biennio un estensione media ottimale del 98,5%.
Premesse Il tumore della mammella rappresenta la neoplasia più frequente ed è ancora la prima causa di morte per tumore nel sesso femminile: si verificano circa 1.000 decessi all’anno, il tasso osservato è stabile, mentre il tasso standardizzato prosegue il trend storico di lieve riduzione. Si stima, sulla base dei dati del Registro Tumori del Veneto (RTV), che nel 2012 in Veneto i nuovi casi di tumore della mammella siano stati 4.425, pari al 32% di tutte le neoplasie nelle donne. Nel 2013 i decessi per questa causa sono stati 95517, il 15% delle morti per tumore nel sesso femminile. Lo screening mammografico è rivolto alle donne fra i 50 e i 69 anni, che in Veneto sono circa 645.000, invitate ad eseguire una mammografia con frequenza biennale. L’obiettivo primario del programma di screening è la riduzione della mortalità specifica per tumore della mammella. Obiettivo secondario è l’applicazione di terapie chirurgiche e mediche il più possibile conservative ed accettabili. Ambedue questi obiettivi sono legati alla individuazione dei tumori quando sono ancora di piccole dimensioni, senza interessamento dei linfonodi e senza metastasi a distanza. Modelli organizzativi Nella realizzazione dello screening mammografico il miglior rapporto costo/benefici è legato all’osservanza del modello organizzativo standard indicato dalle linee guida nazionali ed internazionali. Questo prevede la doppia lettura differita della mammografia (Mx), con il successivo richiamo delle positive/sospette per gli approfondimenti. La doppia lettura viene utilizzata da tutti i programmi della regione. A fine 2013 le ULSS 9, 12, 13, 14 utilizzavano un’unità mobile per la mammografia di primo livello, con lettura differita. Estensione Nel 2013 lo screening mammografico era presente in tutte le ULSS con una popolazione bersaglio di 629.027 donne (dati ISTAT al 01/01/2013). Complessivamente sono state invitate 278.596 donne, pari al 100% della popolazione bersaglio annuale, al netto delle donne escluse prima dell’invito (Tavola 2 in Appendice). A livello delle singole Aziende, tenuto conto delle esclusioni effettuate prima dell’invito, nell’anno 2013, 20 programmi su 21 hanno invitato almeno l’80% delle donne eleggibili (Figura 2). La chiave di lettura più appropriata rimane comunque l’analisi dei risultati di ciascun programma nel tempo. Vi è infine da segnalare che quasi tutti i programmi hanno diversi round organizzativi al loro attivo. Questo implica che in Veneto la maggior parte dell’attività di screening è rappresentata da esami effettuati in donne già screenate in precedenza (155.075, rispetto a 28.560 in donne al primo esame). Inoltre, delle donne ai primi esami, le neo-cinquantenni costituiscono la maggioranza: il 77,4%. Queste considerazioni, come vedremo, sono rilevanti nella interpretazione dei risultati di alcuni indicatori, come l’adesione e la detection rat
Il valore medio regionale dell’adesione corretta nel 2013 (74,5%) non subisce oscillazioni rispetto all’anno precedente, mantenendosi comunque notevolmente superiore alla media dei programmi italiani del 2013 (62,2%) ed in linea con lo standard desiderabile GISMa (75%) (Figura 3). Questo dato, che va interpretato a livello locale, può essere letto come un indicatore di qualità percepita dalle utenti e della conseguente capacità dei programmi di “fidelizzare” le donne che hanno già aderito almeno una volta, vista la quota prevalente di donne agli esami successivi. L’andamento temporale dell’adesione nei singoli programmi denota in alcune ULSS una variabilità che potrebbe riflettere una differenza geografica o anagrafica delle invitate in anni diversi, oppure una quota maggiore di donne invitate ad esami successivi. Qualora le differenze tra due anni successivi siano particolarmente elevate il dato andrebbe verificato localmente.
I tempi della procedura di screening È importante che le donne che aderiscono alla mammografia ricevano una risposta sufficientemente tempestiva, anche se il risultato è normale, ma soprattutto che l’approfondimento diagnostico per le donne positive al test sia effettuato in tempi brevi. In caso di mammografia negativa il 64,3% delle risposte è stato inviato alle donne entro 15 giorni 67 LO SCREENING MAMMOGRAFICO – I RISULTATI DEI PROGRAMMI DI SCREENING 2013 dall’esecuzione del test: il dato non subisce variazioni rispetto al 2012 e resta inferiore allo standard accettabile GISMa (Tabella 2). I programmi che in più del 50% dei casi hanno impiegato più di 15 giorni per l’invio delle risposte sono otto. L’andamento dei tempi di risposta si riflette anche sui tempi di esecuzione degli approfondimenti: di questi il 66% è stato eseguito entro un mese dalla mammografia di screening (il 69% nel 2012, il 57% nel 2011) e solo il 54,6% entro lo standard dei 20 giorni. Si sottolinea però una elevata variabilità tra i programmi. In quattro di questi la percentuale si abbassa al di sotto 30%, ossia più del 70% degli approfondimenti viene eseguito oltre i 28 giorni, con conseguente maggior carico d’ansia per le donne risultate positive (ULSS 6, 9, 14, 17). Anche a livello italiano si riscontra la permanente difficoltà nel raggiungere lo standard desiderabile: nel biennio 2011-12 solo il 71% degli invii degli esiti negativi avviene entro 21 dalla mammografia, mentre solo il 63% degli approfondimenti vengono eseguiti entro 28 giorni dalla mammografia29.
Richiami intermedi Le Linee Guida europee raccomandano di evitare i richiami intermedi conseguenti ad una sessione di primo livello (standard desiderabile: 0%), a causa della bassa probabilità di avere dalla mammografia un quadro più chiaro dopo un intervallo di tempo limitato7 . Andrebbero evitate anche le mammografie eseguite prima dei due anni dopo una sessione di approfondimento negativo (richiami precoci: standard accettabile 10%); permangono però valori inaccettabilmente bassi in alcune ULSS. Pur considerando i limiti dei dati, questi risultati implicano evidenti difformità di comportamento diagnostico tra i diversi programmi. Il rapporto fra lesioni benigne e maligne Questo indicatore si calcola sulle pazienti cui è stata consigliata una verifica chirurgica e deve essere il più basso possibile. Originariamente il suo scopo era quello di monitorare uno dei possibili effetti 70 negativi degli screening, ma l’uso di metodiche diagnostiche microinvasive (agobiopsia, mammotome) al posto delle biopsie chirurgiche ha tolto progressivamente significato a questo indicatore, che dovrà essere sostituito. Infatti sia la media regionale (0,12) che i valori di quasi tutti i programmi rientrano nel valore desiderabile (range 0,00 – 0,38), anche nelle donne 50-54enni (0,23).
Nel 2013, ogni 1.000 donne screenate per la prima volta sono state identificate 6,5 neoplasie, dato in leggero aumento rispetto all’anno precedente ma comunque inferiore allo standard di riferimento
Come l’anno precedente, tredici programmi su ventuno hanno riportato un tasso di identificazione inferiore allo standard di riferimento. Per interpretare questo dato, va ricordato che nella nostra Regione il ricorso alla mammografia spontanea è una pratica diffusa e c’è ragione per ritenere che lo sia maggiormente nelle donne sotto i 50 anni. Quanto più elevata è la quota di donne che si sono sottoposte a mammografie spontanee precedenti il primo esame di screening, tanto meno il primo screening sarà di “prevalenza”, e sarà invece più simile allo screening di “incidenza” dei round successivi. Purtroppo il dato sull’esecuzione di mammografie spontanee fuori dallo screening non è disponibile. Per questi motivi, unitamente al fatto che le donne al primo esame di screening rappresentano solo il 16,8% del totale dell’attività di screening, questo indicatore va considerato meno rilevante e meno rappresentativo della performance diagnostica dei programmi rispetto all’omologo sulle donne agli esami successivi. Complessivamente, il tasso di identificazione negli esami successivi è di poco al di sopra dello standard, tre quarti dei programmi riescono a raggiungerlo, e globalmente risulta di poco superiore rispetto all’anno precedente (Figura 7). La variabilità territoriale del tasso di identificazione dipende non solo dalla sensibilità diagnostica del radiologo, ma anche da altri fattori, tra cui per esempio la diffusione dell’utilizzo della mammografia prima dell’avvio del programma.
Stadio alla diagnosi
I casi trovati allo screening nel 2013 sono 1.105: lo stadio è stato riportato nell’86,6% dei casi, rispetto all’85,6% del 2012 e all’81,5% del 2011. In 148 casi i programmi non hanno ricevuto informazioni (60 casi con stadiazione ignota), oppure i tumori sono risultati non operabili. Si continua a registrare quindi una certa perdita di informazioni. I cancri in situ sono 142 (14,8%). La dimensione del tumore rappresenta un ottimo parametro per predire la probabilità di buon esito della terapia. Lo screening mira ovviamente a identificare lesioni di piccole dimensioni. Degli 804 casi invasivi, 458 (47,9%) avevano dimensione fino a 1 cm, e tra questi 49 erano microinvasivi e 26 avevano diffusione linfonodale. Il tasso di identificazione per i tumori invasivi fino a 10 mm è stato di 1,63 per 1.000 donne esaminate (standard: >1,5 ogni 1.000 donne esaminate). La proporzione di casi identificati allo screening in stadio II o più avanzato è stata del 27,8% ai primi esami e del 27,1% a quelli successivi (standard desiderabile6 :
Trattamento chirurgico nei tumori invasivi
La correlazione tra pT e tipo di intervento chirurgico (conservativo/radicale, con/senza dissezione ascellare) è stata riportata per 821 tumori invasivi. Nell’81,6% dei casi (n = 670) si tratta di tumori invasivi ≥ 2 cm (85,3% nel 2012, 84% nel 2011). I trattamenti riportati sono stati prevalentemente conservativi (80,5% nel 2013 e 82,4% nel 2012) con o senza dissezione ascellare, coerentemente con l’elevata proporzione di lesioni di basso stadio. Come atteso e coerentemente con una distribuzione più favorevole delle dimensioni delle lesioni, i trattamenti conservativi sono risultati più frequenti negli esami successivi, rispetto ai primi esami (82,8% rispetto al 70,6%).
Conclusioni
Si riassumuno i più rilevanti indicatori di qualità dello screening mammografico della Regione Veneto per il periodo 2011-2013, con gli standard di riferimento definiti dal GISMa. Nel 2013 l’estensione media migliora nettamente rispetto ai valori ottenuti negli anni precedenti. Permangono tuttavia delle difficoltà nel mantenere e, dove necessario, aumentare i volumi di lavoro in circa un quinto delle ULSS. Il dato dell’adesione corretta non subisce variazioni rispetto al 2012, si posiziona leggermente al di sotto dello standard desiderabile del 75%, ma riesce comunque a mantenere lo scarto di miglioramento rispetto al 2010 e a mantenersi superiore alla media nazionale. Il tasso di richiamo ai primi esami aumenta di un punto e mezzo percentuale, continuando ad essere superiore allo standard accettabile. Agli esami successivi il tasso di richiamo si attesta agli stessi livelli dell’anno precedente. Si conferma l’andamento virtuoso di diminuzione dei richiami intermedi, come raccomandato dalle Linee Guida Europee che ne sconsigliano l’utilizzo. I tempi con cui i programmi inviano la risposta negativa non registrano variazioni sostanziali nel 2013, mentre continuano a migliorare i tempi di invio ad approfondimento. Questo dato, che potrebbe essere legato ad una revisione degli aspetti organizzativi nei richiami all’approfondimento, va confermato nei prossimi anni. Nel 2013 i tumori screen detected sono stati 1.105. Come nell’anno precedente, il tasso di identificazione agli esami successivi soddisfa lo standard di riferimento, mentre ai primi esami rimane inferiore, ma con un netto miglioramento rispetto agli anni precedenti. Una possibile spiegazione sta nel frequente ricorso alla mammografia nelle donne < 50 anni.
Complessivamente, gli indicatori risultano soddisfacenti nel confronto con gli standard nazionali, e stabili rispetto all’anno precedente. Ognuno di essi però deriva dalla composizione di valori molto variegati nelle diverse ULSS, cui si rimanda per una più adeguata valutazione delle realtà locali. Con l’adozione della doppia lettura da parte di tutte le ULSS, diminuisce la difformità dei modelli organizzativi e dei percorsi diagnostici, che comporta un uso poco efficiente della risorsa più scarsa, cioè il tempo-radiologo. Alcune realtà soffrono ancora nel garantire il reinvito a due anni a tutta la popolazione di riferimento, mentre in altre il recupero dei dati relativi agli approfondimenti e agli interventi risulta ancora di difficile attuazione